Phone 17’nin lansmanı yaklaşırken, Apple’ın yapay zekâdaki ilerlemesi beklendiği kadar hızlı değil. “Bir yandan güçlü...
Antikorların ve T hücresi reseptörlerinin tamamlayıcılık belirleyici bölgelerinin konformasyonel esnekliğinin tahmin edilmesi
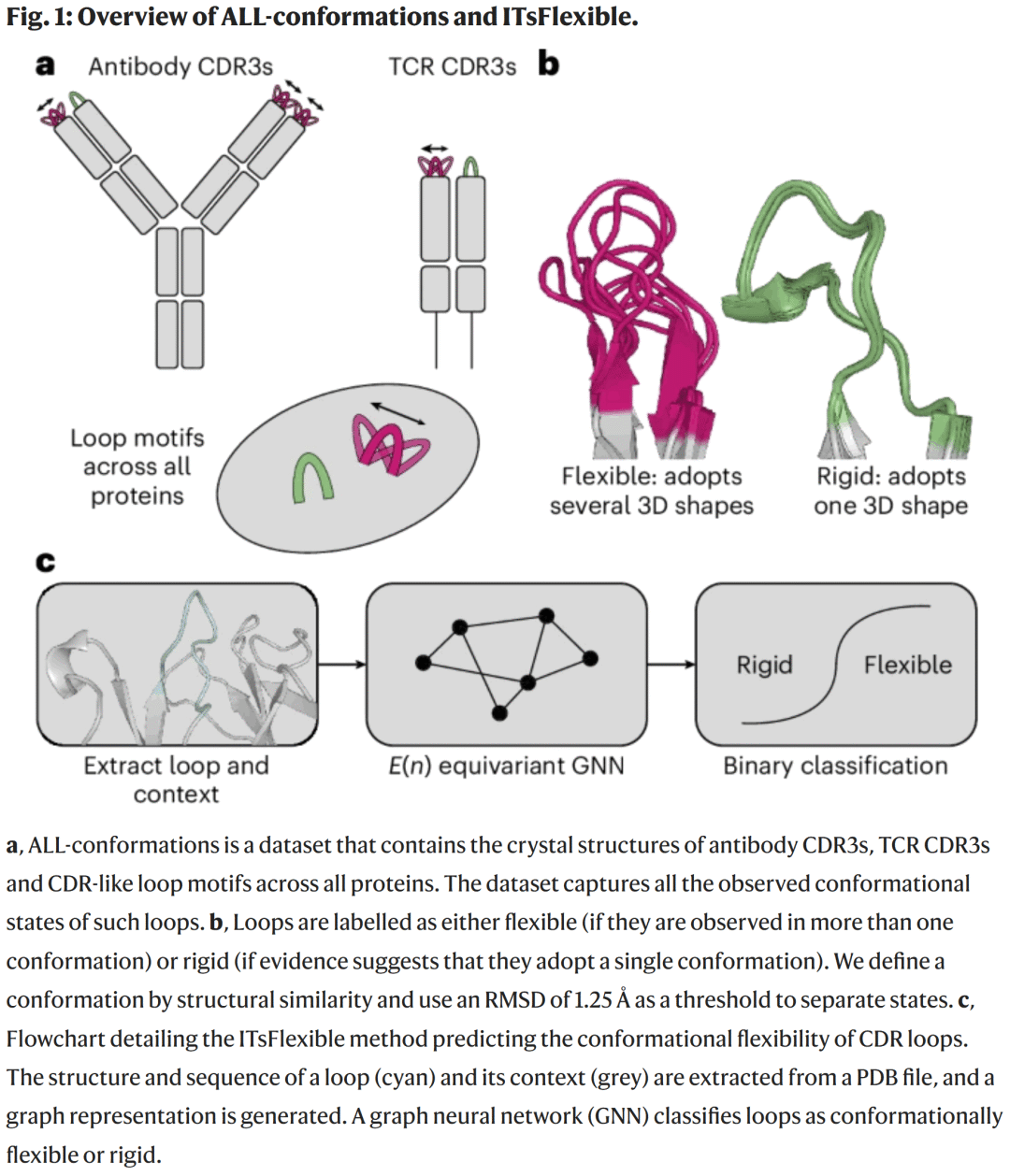
Proteinler yüksek derecede konformasyonel esnekliğe sahiptir ve şekle uyum sağlama yetenekleri fonksiyonel özellikler açısından kritik öneme sahiptir. Örneğin, antikor tamamlayıcılığını belirleyen bölge (CDR) döngülerinin esnekliği, bağlanma afinitesini ve özgüllüğünü etkiler ve antijen bağlama yeteneklerinin anlaşılmasında ve tasarlanmasında anahtar bir faktördür. AlphaFold gibi yöntemler tek statik yapıları yüksek doğrulukla tahmin edebilse de, esas olarak uygun eğitim verilerinin kıtlığı nedeniyle yapısal esnekliğin güvenilir tahmini sağlanamamıştır.
Araştırmacılar, antikorlar ve T hücresi reseptörlerindeki (TCR’ler) işlevsel açıdan önemli CDR3 döngüsündeki esnekliğin tahmin edilmesine odaklandı. Bu amaçla, araştırmacılar ALL konformasyonları veri setini oluşturdular ve CDR3 ve benzer halka yapılarını Protein Veritabanından (PDB) sistematik olarak çıkardılar. Deneylerde gözlemlenen tüm konformasyonları kapsayan toplam 1,2 milyon halka yapısı ve 100.000’den fazla benzersiz dizi içerir. Bu veri setine dayanarak araştırmacılar, CDR halkalarını “katı” veya “esnek” olarak sınıflandırabilen, grafik sinir ağlarına (GNN) dayalı bir derin öğrenme aracı olan ITsFlexible modelini geliştirdiler. ITsFlexible, kristal yapı veri setleri üzerindeki tüm kontrol yöntemlerinden daha iyi performans gösterir ve moleküler dinamik simülasyonlarına genellenir. Araştırmacılar ayrıca, çözülmüş yapılar olmadan üç CDRH3 döngüsünün esnekliğini tahmin etmek için ITsFlexible’ı kullandı ve bunları kriyo-elektron mikroskobu deneyleriyle doğruladı. Tahmin sonuçlarından ikisi deneylerle tutarlıydı.

Proteinler sıklıkla birden fazla kararlı konformasyonel duruma sahiptir ve bu durumlar arasındaki geçişler fonksiyon için kritik öneme sahiptir. Antikorlar ve TCR’ler esas olarak antijenleri, konformasyonel esnekliği bağlanma özgüllüğünü, afinitesini ve çoklu özgüllüğü etkileyen altı tamamlayıcılık belirleyici bölge (CDR’ler) aracılığıyla tanır. Esneklik bağlanma spektrumunun genişliğini arttırabilir ancak afiniteyi de azaltabilir.
AlphaFold gibi modeller statik yapıları doğru bir şekilde tahmin edebilse de, proteinlerin çoklu konformasyonel durumlarını tahmin etmek son derece zorlu olmaya devam ediyor. Zorluğa neden olan önemli bir faktör, eğitim için mevcut yüksek kaliteli verilerin eksikliğidir. Nükleer manyetik rezonans (NMR) ve hidrojen-döteryum değişim kütle spektrometresi gibi deneysel teknikler dinamikleri ölçebilse de atom düzeyinde esneklik bilgisi elde etmek zordur; kristal yapılar yüksek çözünürlüklü olmasına rağmen konformasyonun yalnızca bir kısmını temsil edebilir. Moleküler dinamik (MD) simülasyonları konformasyonel topluluklar oluşturabilir ancak hesaplama açısından pahalıdır ve büyük ölçekli makine öğrenimi modeli eğitimini desteklemek için henüz yeterli değildir.
Bu bağlamda araştırmacılar, veri eksikliğini gidermek için proteinin tamamını kapsayan bir halka yapısı veri tabanı oluşturarak antikorların ve TCR’lerin CDR3 esnek tahminine odaklanıyor ve böylece genelleştirilebilir esnek bir tahmin yöntemi geliştiriyor.
Yönteme genel bakış
ALL uyumlu veri seti yapısı
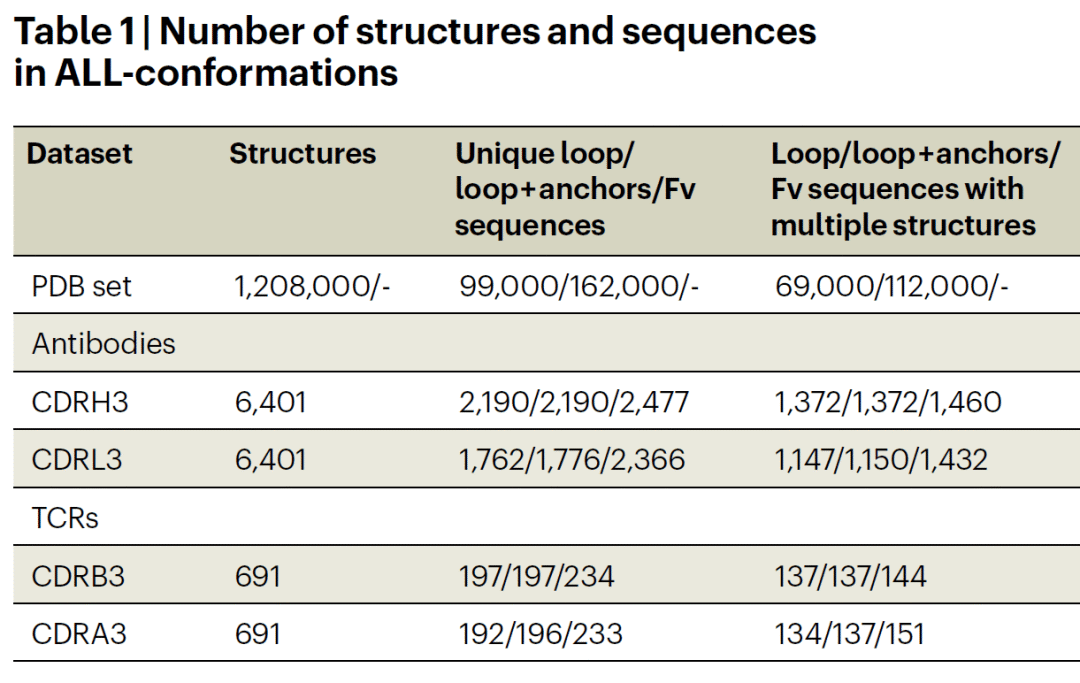
Araştırmacılar, beş alt küme içeren ALL konformasyon veri setini oluşturmak için PDB’den iki antiparalel β-iplikçik ile çevrelenmiş halka yapılarını sistematik olarak incelediler: antikorlar CDRH3, CDRL3, TCR CDRB3, CDRA3 ve tüm proteinlerdeki benzer halka yapıları. Veri seti, deneysel olarak gözlemlenen tüm konformasyonel durumları kapsayan toplam 1,2 milyon kristal yapı ve yaklaşık 100.000 benzersiz dizi içerir.
Döngüler “esnek” veya “sert” olarak tanımlandı: aynı dizi, farklı yapılarda birden fazla konformasyonda görünüyorsa esnek, en az beş bağımsız kristal yapıda tutarlıysa katı olarak etiketlendi. Sonuçta 16.000’den fazla sert halka ve 4.000’den fazla esnek halka ortaya çıktı.
BTEsnek model tasarımı
ITsFlexible, E(n)-eşdeğer grafik sinir ağını (GNN) temel alan ikili bir sınıflandırma modelidir. Girdi, halkaların ve bunların yerel yapısal ortamlarının grafik gösterimlerini içerir. Düğüm özellikleri, bir halkaya ait olup olmadığı, Cα atomik koordinatları vb. gibi amino asit türünü kodlar; kenar özellikleri kovalent bağ bilgilerini ve mesafe kodlamasını içerir. Model, düğüm temsilini üç grafik evrişim katmanı aracılığıyla günceller ve doğrusal katmanlar aracılığıyla esnek olasılıklar üretir.
Model, ikili çapraz entropi kaybı fonksiyonu ve Adam optimizer kullanılarak, eğitim-doğrulama-test oranı 70–15–15 olacak şekilde eğitildi ve dizi benzerliği %80’i geçmeyecek şekilde kontrol edildi.
Temel ve kontrol yöntemleri
Karşılaştırmalı modeller şunları içerir:
-
Halka uzunluğu ve solvent maruziyetine dayalı lojistik regresyon modeli;
-
AlphaFold tarafından tahmin edilen kalıntı güvenirliği (pLDDT) modeli;
-
AlphaFold, çoklu dizi hizalama (MSA) alt örneklemesine dayalı konformasyonel çeşitlilik yöntemi oluşturur;
-
Antikor spesifik öngörücü ABodyBuilder2’nin RMSPE (tahmin hatası) göstergesi.
sonuç
ALL-konformasyon veri seti analizi
Bu veri seti, proteinlerdeki β-şerit halka yapılarının tüm deneysel konformasyonlarını kapsamlı bir şekilde yakalar. Araştırmacılar halkaların esneklik özelliklerini etiketlemek için RMSD kümeleme yöntemini kullandılar ve sonunda net esneklik etiketlerine sahip 20.000’den fazla halka dizisi elde ettiler.
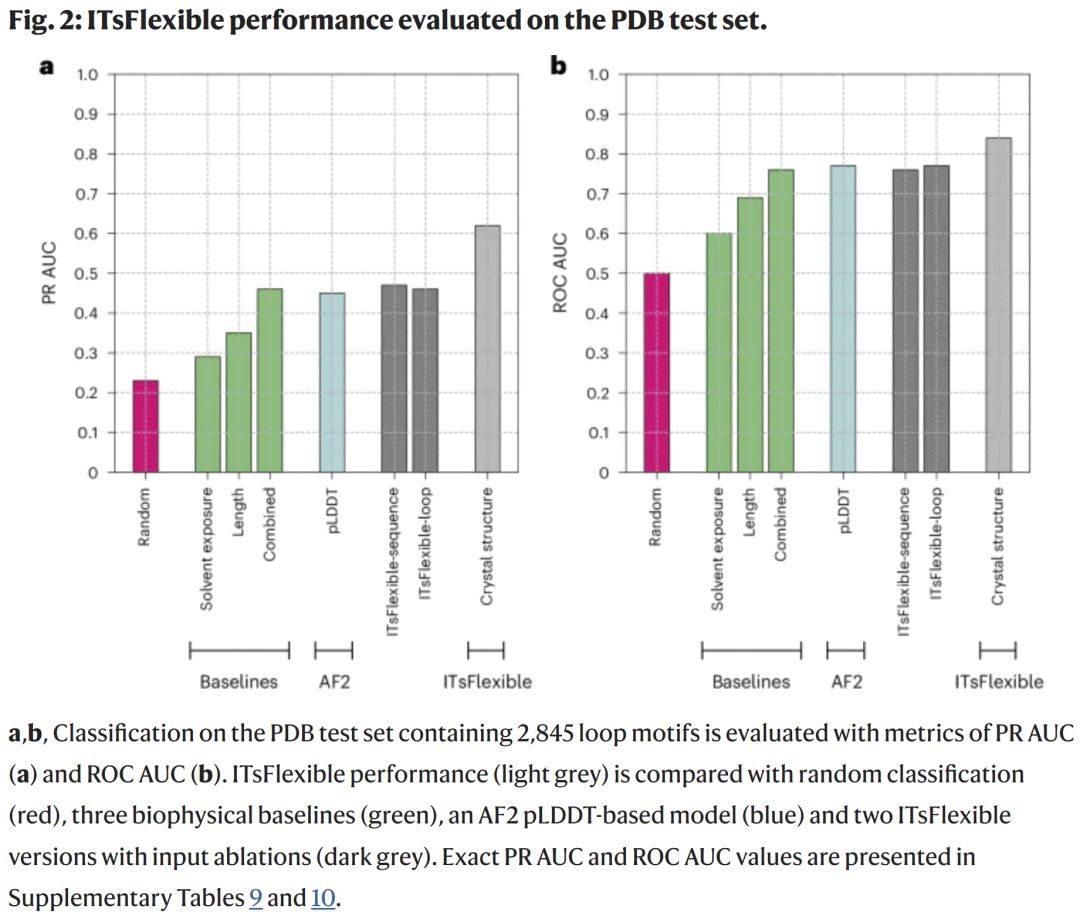
Model performans değerlendirmesi
PDB test setinde, ITsFlexible’ın ROC AUC’si 0,84’e ulaşır ve PR AUC’si 0,62’dir; bu, tüm temel ve sıfır numune yöntemlerinden önemli ölçüde daha iyidir (Şekil 2). Model ablasyon deneyleri, yalnızca döngü dizileri veya yerel yapılar kullanan modellerin performansının düştüğünü gösteriyor, bu da döngülerin çevreleriyle etkileşiminin esnekliğin önemli bir belirleyicisi olduğunu gösteriyor.
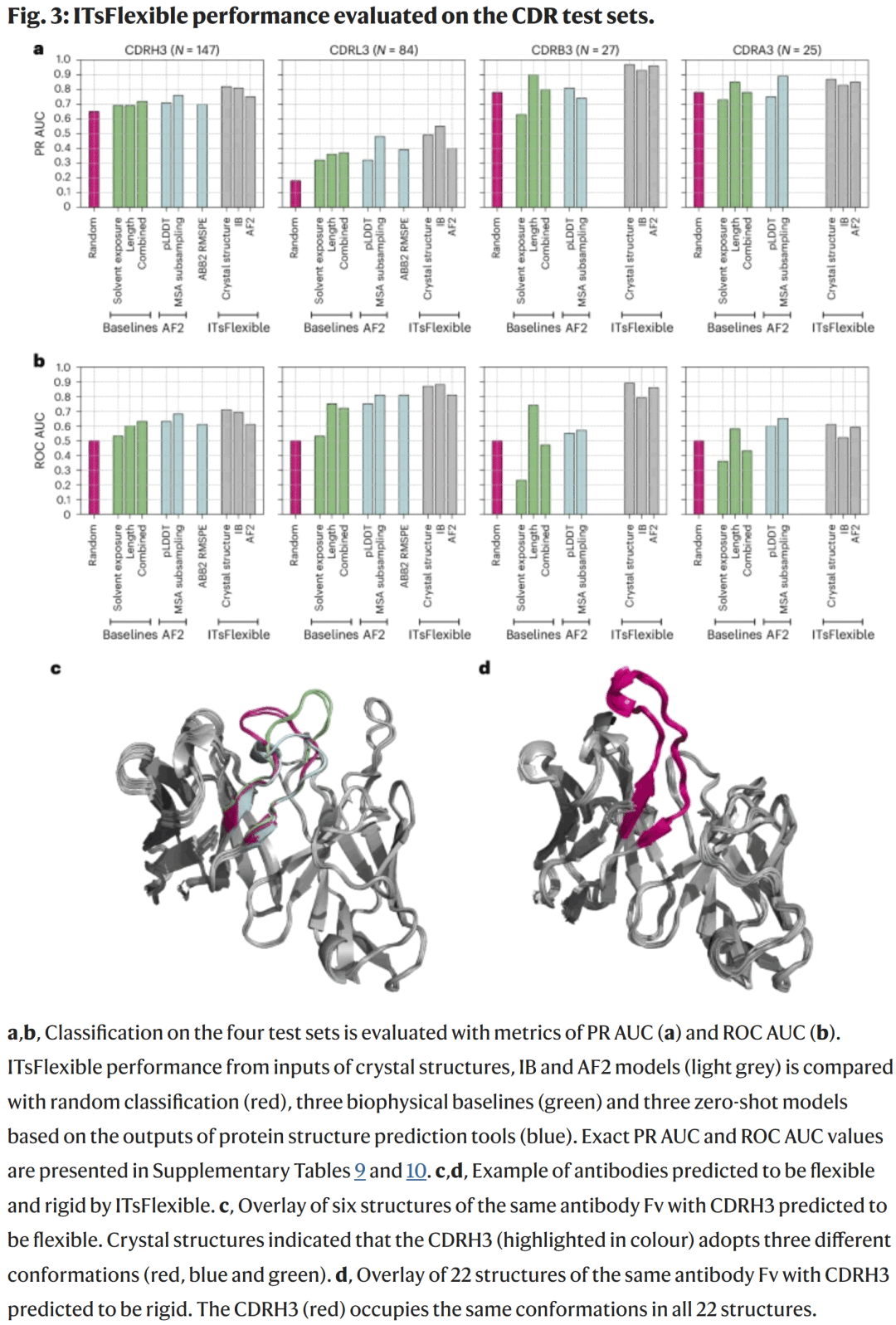
Antikorların ve TCR’lerin esnek tahmini
Araştırmacılar ayrıca antikorların ve TCR’lerin CDR3 verileri üzerindeki model performansını değerlendirdi. ITsFlexible, özellikle en iyi performansı gösteren ve AlphaFold MSA alt örnekleme ve ABodyBuilder2 tahmin hatası modellerinden daha iyi performans gösteren CDRH3 setinde, dört CDR tipinin tamamı (H3, L3, A3, B3) (Şekil 3) için yüksek doğruluk elde eder.
Sonuçlar şunu gösteriyor:
-
CDRL3 ve CDRB3 en doğru şekilde sınıflandırılmıştır;
-
CDRH3 biraz daha düşük performansa sahiptir ancak yine de tüm yöntemlere öncülük etmektedir;
-
Model, yüksek dizi çeşitliliğinde bile istikrarlı genelleme yeteneğini korur.
Moleküler Dinamik Doğrulaması
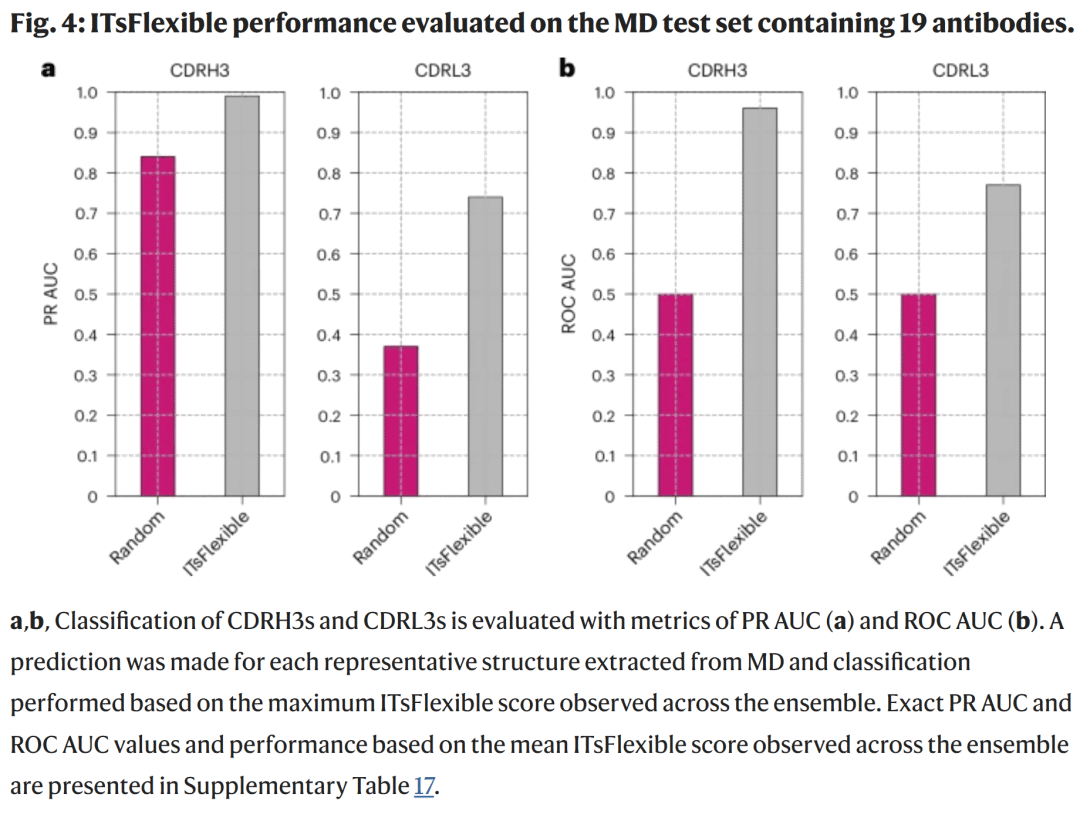
Araştırmacılar, CDR3’ün esnek etiketlerini bağımsız olarak hesaplamak için 19 antikor üzerinde MD simülasyonları gerçekleştirdi. Sonuçlar şunu gösteriyor:
-
MD verilerinde CDRH3’ün esneklik oranı %84, CDRL3’ün ise %37;
-
ITsFlexible, esnek ve sert halkalar arasında doğru bir şekilde ayrım yaparak mükemmele yakın bir ayrım gösterir.
Kriyo-elektron mikroskobu deneysel doğrulaması
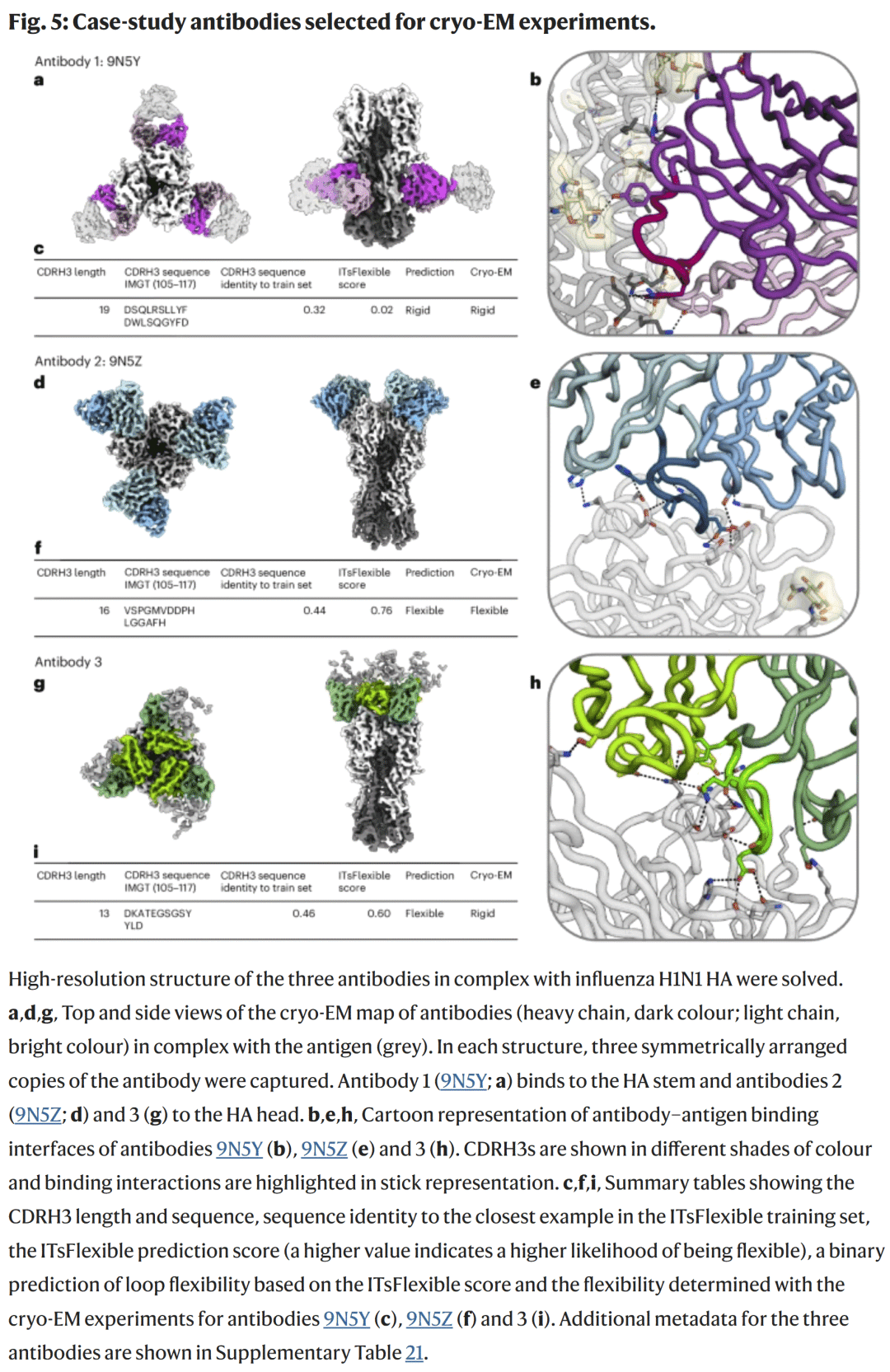
Araştırmacılar, kriyo-EM doğrulaması için farklı tahmin edilen sonuçlara sahip üç antikor seçtiler.
-
Antikor 1: Sert olduğu tahmin edilen deney, tahminle tutarlı olarak tek bir konformasyon gösterdi;
-
Antikor 2: Esnek olduğu tahmin edildi, bağlanma arayüzünde deneysel olarak gözlemlenen konformasyonel heterojenlik, doğru olduğu doğrulandı;
-
Antikor 3: Esnek olduğu tahmin edildi, ancak deneysel olarak hiçbir heterojenlik gözlenmedi, muhtemelen antijen bağlanması nedeniyle sertleşmeye neden oldu.
Genel olarak, her iki tahmin de deneylerle tutarlı olup, modelin güvenilirliğini doğrulamaktadır.
tartışmak
Konformasyonel değişiklikler, özellikle antikorlar ve TCR’ler için birçok protein fonksiyonunun merkezinde yer alır. CDR3’ün esnekliği bağlanma afinitesini ve özgüllüğünü doğrudan etkiler. Ancak mevcut yapı tahmin araçları birden fazla konfigürasyonu yakalamakta zorlanıyor.
Araştırmacılar ALL-konformasyon veri setini ve ITsFlexible modelini oluşturarak CDR3 esnekliğinin yüksek hassasiyetli tahminini elde etti. Bu yöntem şunları ortaya çıkarır:
-
Sıra ve yerel yapısal çevre, halkanın esnekliğini birlikte belirler;
-
Model, deneysel yapısı olmayan antikorlarda tahmine dayalı model girdilerini kullanarak güvenilir karar verilmesini sağlar;
-
Ne AlphaFold güveni (pLDDT) ne de antikor tahmin hatası (RMSPE) esnekliği karakterize etmek için yeterli değildir;
-
MSA alt örneklemesi yapısal çeşitliliği artırabilse de, yine de gerçek konformasyonel esnekliği doğru şekilde yansıtamaz.
Ayrıca araştırmacılar, modelin ilaç tasarımına yardımcı olabileceğine dikkat çekti:
-
Esnek tahmin, daha yüksek afinite ve spesifikliğe sahip antikorların taranmasına yardımcı olabilir;
-
Bilgisayar kaynağı kullanımını iyileştirmek için MD simülasyonu gerektiren moleküllere öncelik verilebilir;
-
Antijen-antikor yerleştirme ve afinite optimizasyonu gibi sonraki görevlerin geliştirilmesine yardımcı olur.
Son olarak araştırmacılar, bu çalışmanın protein esneklik modellemesi için bir temel oluşturduğuna inanıyor; bu model, gelecekte bağlı ve serbest durum konformasyonlarının karşılaştırmalı tahminine kadar genişletilebilir ve biyomolekül tasarımı için yeni bir araç yolu sağlayabilir.
Referanslar
Spoendlin, FC, Fernández-Quintero, ML, Raghavan, SSR ve diğerleri. Antikor ve T hücresi reseptörü tamamlayıcılığını belirleyen bölgelerin konformasyonel esnekliğinin tahmin edilmesi. Nat Mach Intel’in (2025).
https://doi.org/10.1038/s42256-025-01131-6

İçerik[AiHaber]e aittir.|Yeniden basarken lütfen kaynağı belirtin
İçerikte yer alan resimler telif hakkı sorunları içeriyorsa lütfen bunları silmek için zamanında bizimle iletişime geçin.




























